
进口三类体外诊断试剂注册证(许可事项变更)服务
《体外诊断试剂注册管理办法》明确规定, 注册证及附件载明内容中发生发生进口体外诊断试剂生产地址变更的,申请人应当向原注册部门申请许可事项变更。 进口三类IVD注册证申请...
服务价:¥电议
好评系数:

《体外诊断试剂注册管理办法》明确规定, 注册证及附件载明内容中发生发生进口体外诊断试剂生产地址变更的,申请人应当向原注册部门申请许可事项变更。
进口三类IVD注册证申请变更(许可事项变更),需填写进口体外诊断试剂注册变更申请表。办理进口三类体外诊断试剂注册变更,需向药监总局相关部门申请、携带相关文件。
《进口IVD注册变更申请表》可变更的许可事项类型有
1、变更抗原、抗体等主要材料的供应商;
2、变更检测条件、阳性判断值或参考区间;
3、变更产品储存条件和/或有效期;
4、修改产品技术要求,但不降低产品有效性的变更;
5、进口体外诊断试剂生产地址的变更;
6、对产品说明书和/或产品技术要求中文字的修改,但不涉及技术内容的更改;
7、变更包装规格;
8、变更适用机型;
9、增加临床适应症;
10、增加临床测定用样本类型的变更;
11、其他可能影响产品有效性的变更。
除了进口IVD注册变更申请表,还要附材料
1、注册人关于变更情况的声明;
2、原医疗器械注册证及其附件复印件;
3、历次医疗器械注册变更文件复印件;
4、具体变更情况的其他技术资料要求:
(1)变更抗原、抗体等主要材料的供应商相应资料;
(2)变更检测条件、阳性判断值或参考区间相应资料;
(3)变更产品储存条件和/或有效期相应资料;
(4)修改产品技术要求,但不降低产品有效性的变更相应资料;
(5)进口体外诊断试剂生产地址的变更相应资料;
(6)对产品说明书和/或产品技术要求中文字的修改,但不涉及技术内容的更改相应资料;
(7)变更包装规格相应资料;
(8)变更适用机型相应资料;
(9)增加临床适应症相应资料;
(10)增加临床测定用样本类型的变更相应资料;
(11)其他可能影响产品有效性的变更相应资料;
应当根据产品具体变更情况,提交该变更对产品性能可能产生的影响进行验证的试验资料(如涉及)。
5、境外申请人注册地或生产地址所在国家(地区)主管部门出具的批准变更的证明文件;
6、境外申请人在中国境内指定代理人的委托书;
7、代理人承诺书;
8、代理人营业执照副本或者机构登记证明复印件;
9、符合性声明和符合标准的清单;
10、申请人所在地公证机构出具的关于英文/原文资料公证件。
进口三类IVD注册证(许可事项变更)服务流程
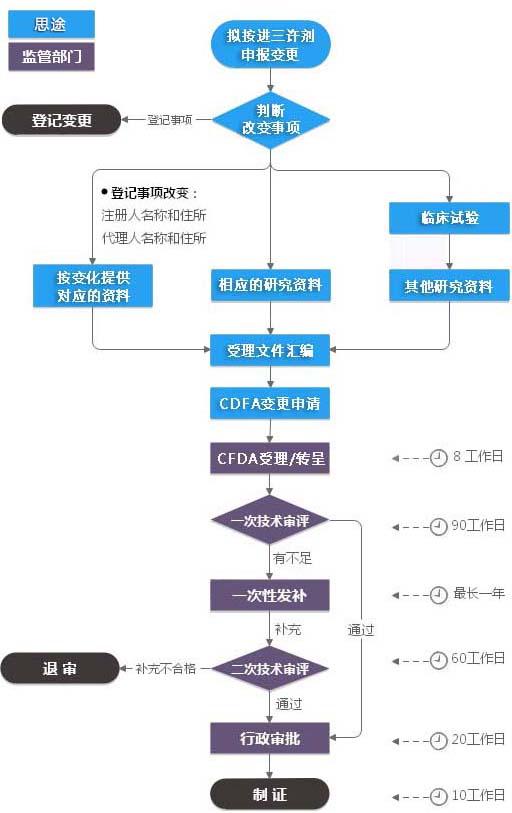
进口三类IVD注册证(许可事项变更)收费标准
| 主管部门 | 产品 | 管理类别 | 首次注册 | 注册变更 (许可事项变更) | 延续注册 |
|---|---|---|---|---|---|
| 国家局(境外) | IVD | Ⅲ | 30.88 | 5.04 | 4.08 |
单位:万元
进口三类IVD注册证(许可事项变更)办理依据
| 文件名称 | 文号 |
|---|---|
| 《医疗器械监督管理条例》 | 650号文件 |
| 《体外诊断试剂注册管理办法》 | 局令5号 |
| 关于印发境内第三类和进口医疗器械注册审批操作规范 | 食药监械管〔2014〕208号 |
| 关于公布体外诊断试剂注册申报资料要求和批准证明文件格式的公告 | 2014年44号 |
进口三类IVD注册证(许可事项变更)服务周期
立项阶段
预算、合同、考虑期,1个月。
受理前资料准备
资料提供、翻译及公证 1-2个月
*如需:产品检测,视产品情况有所变化。 *平均6个月
*如需:临床试验不可与检测并行,临床应单独核算时间。 *至少9个月
变更资料编制(可与检测或临床并行。) 1个月
受理后
CFDA法定消耗预算7个月。(128工日,20工日/月,不计节假) 至少7个月
*发补(如适用):1、发补资料准备时限0~12个月视产品递交的申报资料情况而定。 *平均6个月
*发补(如适用):2、发补技术评审时间预计消耗3个月(60工作日) *3个月
*如需:体系考核,注册受理后,额外30工作日 *1.5个月
预算合计
无需重新检测、临床、体考、发补 预算平均11个月
进口三类IVD注册证(许可事项变更)推荐服务
| 进口三类IVD首次注册代办服务 | 进口创新医疗器械申报服务 |
| 进口第三类IVD注册(登记事项变更)服务 | ivd临床试验服务 |
 最新文章
最新文章 2024-04-26
2024-04-26 2024-04-24
2024-04-24 2024-04-24
2024-04-24 2024-04-22
2024-04-22 2024-04-19
2024-04-19八年
医疗器械服务经验
-
多一份参考,总有益处
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台
- 在线咨询
- 在线客服
- 服务热线
服务热线
186-0382-3910
- 微信咨询

- 返回顶部












 豫公网安备 41010202003160号
豫公网安备 41010202003160号