药械组合产品属性界定申请资料和流程图
来源:医疗器械注册代办 发布日期:2023-10-10 阅读量:次
本文源自《关于调整药械组合产品属性界定有关事项的通告(2019年第28号)》附件:药械组合产品属性界定工作流程,如果您对自家新研发产品无法判定是医疗器械?是药物?还是药械组合?您可以依据以下方式申请进行药械组合产品属性界定。

一、申请方式
申请人通过中国食品药品检定研究院(国家药品监督管理局医疗器械标准管理中心)网站(网址:http://www.nifdc.org.cn/)进入“医疗器械标准管理中心”二级网站(网址:https://www.nifdc.org.cn/nifdc/bshff/ylqxbzhgl/index.html),点击进入“药械组合产品属性界定信息系统”,填写《药械组合产品属性界定申请表》,并上传其他申请资料。
二、申请资料要求
(一)药械组合产品属性界定申请表
(二)支持性材料
1.产品描述
产品的名称、组成成分(所含成分剂量)、组合方式、预期用途、使用时与患者接触部位/接触时间、产品示意图、实物照片等。
2.作用机制
组合产品及各组成成分的作用机制,主要及次要作用方式,并提供相关的支持和验证性资料。
3.拟采用的使用说明书(或用户手册等)
4.组合产品各组成成分来源
5.申请人属性界定意见及论证资料
组合产品实现预期目的的首要作用方式、确定依据和支持性试验资料及文献资料,对组合产品中发挥、部分发挥和不发挥主要作用的组分进行系统论证并提供支持性资料。
6.相关产品的描述及监管情况
明确药械组合产品中药品或组分按药品管理及其佐证资料。如已有相似或相关的产品在境内或境外上市,简要介绍该产品结构、组成(含量)、预期用途等基本情况、管理属性和类别及支持性资料。对于境外产品属性界定申请,应同时提交该组合产品在其当地上市的资料。
7.其他与产品属性确定有关的资料
在线打印《药械组合产品属性界定申请表》并签字签章,扫描后连同其他申请资料一并按要求上传。所有申请资料应当使用中文。根据外文资料翻译的,应当同时提供原文。
三、申请状态和结果查询
申请人登陆“药械组合产品属性界定信息系统”即可查询申请状态和结果。
网址:http://app.nifdc.org.cn/biaogzx/login.do?formAction=login&yxzh=yxzh
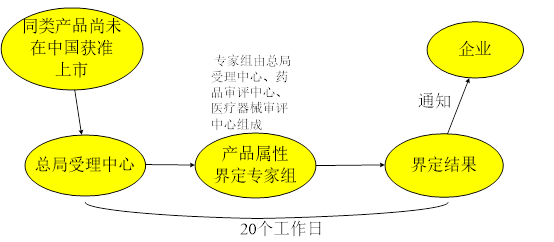
四、药械组合产品属性界定流程

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
郑州思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
行业资讯
知识分享









 豫公网安备 41010202003160号
豫公网安备 41010202003160号