谈谈医疗器械产品的寿命界定方法
来源:医疗器械注册代办 发布日期:2023-10-10 阅读量:次
前言:医疗器械的使用寿命是指医疗器械从规划、设计、生产、销售、安装调试到使用、维修、维护检测、报废的全过程。而医院使用的医疗器械的应用质量和安全管理在整个寿命过程中占重要地位。
根据现行法规、产品上市情况,对医疗器械产品的寿命界定方法做以下简单总结:
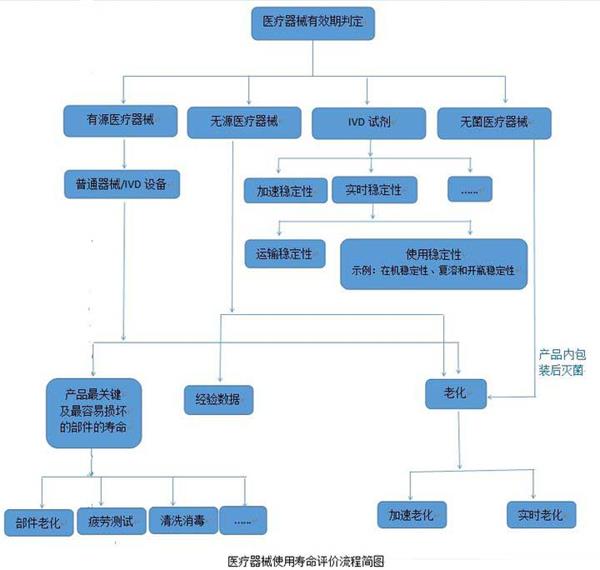
需要注意的是,加速老化包括部件老化和整机老化,有源医疗器械受使用环境、使用条件的影响较大,一般不采用整机实时老化,比如一台电脑,放置5年不使用跟一直使用5年的结果肯定不一样,对于结构相对简单的、寿命较短的器械比较适用。无菌产品的老化必须在产品内包装后灭菌再进行,且实时稳定性试验和加速稳定性试验应同时进行,实时稳定性试验结果是验证产品货架有效期的直接证据。当加速稳定性试验结果与其不一致时,应以实时稳定性试验结果为准。
目前医疗器械有效期评价方法可参考引用的标准有以下:
YY/T 0681.1-2009 无菌医疗器械包装试验方法 第1部分 加速老化试验指南
2017年第75号 无源植入性医疗器械货架有效期注册申报资料指导原则(2017年修订版)
ASTM F 1980-2002 无菌医疗设备包装加速老化标准指南
YY/T 1579-2018 体外诊断医疗器械体外诊断试剂稳定性评价
2018年09月29日 《有源医疗器械使用期限技术审查指导原则(征求意见稿)》
参考:
1《有源医疗器械使用期限技术审查指导原则(征求意见稿)》
2 体外诊断试剂产品有效期的确定-审评六部 供稿
3 浅谈医疗器械有效期的持续研究-作者:CIO合规保证组织 黄绍乐
4 浅谈提高医疗器械使用寿命的见解-江门市开平中医院设备科 谭丹华
5《无源植入性医疗器械货架有效期注册申报资料指导原则(2017年修订版)》

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
郑州思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
行业资讯
知识分享









 豫公网安备 41010202003160号
豫公网安备 41010202003160号